Укажите ряд, в котором приведены формулы двух сложных и одного простого вещества:
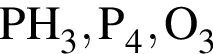
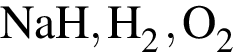
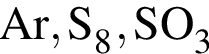
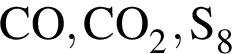
Укажите ряд, в котором приведены формулы двух сложных и одного простого вещества:
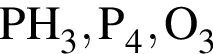
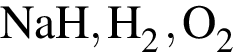
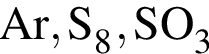
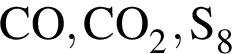
Заряд ядра атома хрома равен:
Электронная конфигурация 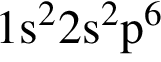 соответствует иону или атому в основном состоянии:
соответствует иону или атому в основном состоянии:
Названия аллотропных модификаций одного и того же химического элемента представлены в ряду:
Пользуясь справочными материалами, предложенными в сборнике тестов, НЕВОЗМОЖНО вычислить молярную массу:
Наибольшее значение степени окисления атомы хлора имеют в соединении:
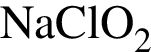
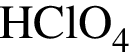
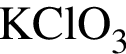
Укажите ряд, в котором оба гидроксида можно получить растворением соответствующего металла в воде:
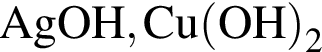
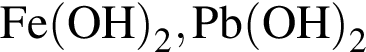
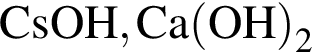
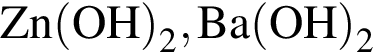
Простое вещество, в реакции с которым водород является окислителем:
Укажите правильное утверждение относительно азота и фосфора:
Для получения железа из водного раствора сульфата железа (II) нецелесообразно использовать металл:
Вещество, водный раствор которого может одновременно являться и разбавленным, и насыщенным, — это:
Основные свойства высших оксидов предложенных элементов монотонно усиливаются в ряду:
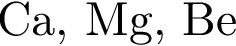
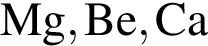
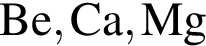
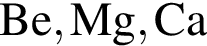
Ионные связи содержатся во всех веществах ряда:
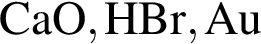
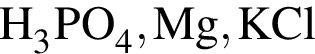
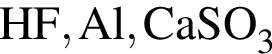
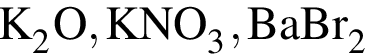
Укажите правильные утверждения относительно вещества, химическая формула которого 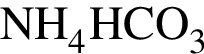 :
:
а — cлабый электролит
б — является кислой солью
в — имеет название карбонат аммония
г — мольное отношение катионов и анионов в формульной единице 1 : 1
При комнатной температуре с водой реагирует вещество:
Углекислый газ образуется в результате реакции, схема которой:
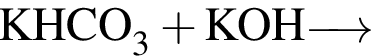
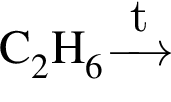
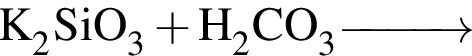
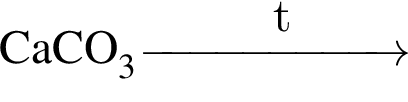
Общее число веществ из предложенных — 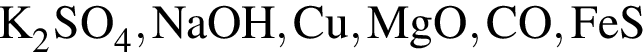 с которыми при комнатной температуре реагирует разбавленная соляная кислота равно:
с которыми при комнатной температуре реагирует разбавленная соляная кислота равно:
Выберите правильное утверждение:
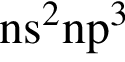
Аммиак является одним из продуктов реакции, схема которой:
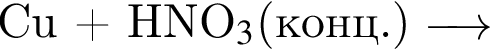
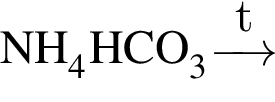
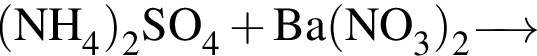

Разбавленная серная кислота реагирует с веществами (электролиты взяты в виде водных растворов):
а — ![]()
б — ![]()
в — ![]()
г — ![]()
Укажите число возможных попарных взаимодействий между веществами 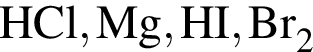 (электролиты взяты в виде водных растворов; возможность химической реакции веществ с растворителем НЕ учитывайте):
(электролиты взяты в виде водных растворов; возможность химической реакции веществ с растворителем НЕ учитывайте):
![]() водного раствора увеличивается при:
водного раствора увеличивается при:
В сосуде объемом 5 дм3 протекает реакция 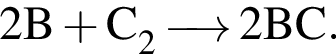 Через 10 с после начала реакции образовалось вещество
Через 10 с после начала реакции образовалось вещество ![]() химическим количеством 20 моль. Средняя скорость (моль/дм3 · с) образования вещества
химическим количеством 20 моль. Средняя скорость (моль/дм3 · с) образования вещества ![]() равна:
равна:
Окислительно-восстановительной реакцией является реакция, схема которой:
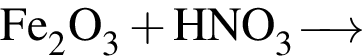
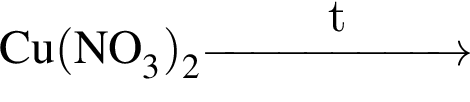
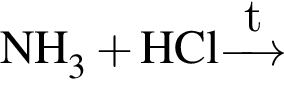
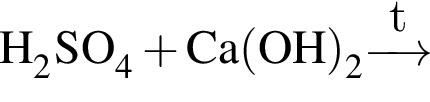
Установите соответствие между веществом и реактивом, который можно использовать для его качественного определения. Bce электролиты взяты в виде водных растворов.
1 — 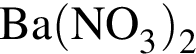
2 — 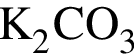
а — ![]()
б — ![]()
в — 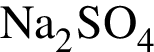
г — ![]()
К раствору азотной кислоты, масса ![]() в котором равна 28,35 г, добавили избыток гидрокарбоната натрия. Если выход газообразного (н. у.) продукта реакции составляет 70%, то его объем (дм3, н. у.) равен:
в котором равна 28,35 г, добавили избыток гидрокарбоната натрия. Если выход газообразного (н. у.) продукта реакции составляет 70%, то его объем (дм3, н. у.) равен:
Правая часть сокращенного ионного уравнения имеет вид... 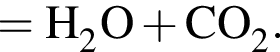
Это соответствует взаимодействию реагентов:
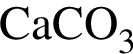 и
и 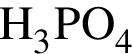
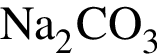 и
и 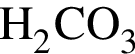
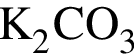 и
и 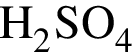
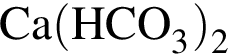 и
и 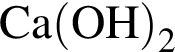
Укажите процесс, одним из продуктов которого является кислород:
Формула насыщенной одноосновной карбоновой кислоты:
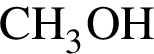
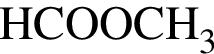
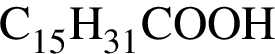
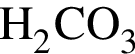
Сумма коэффициентов перед продуктами в уравнении химической реакции полного сгорания бутана равна:
Вещество, которое НЕ вступает в реакцию гидрирования, — это:
Веществу 2-метилпентановая кислота соответствует формула:
Укажите схему реакции отщепления согласно классификации органических реакций:
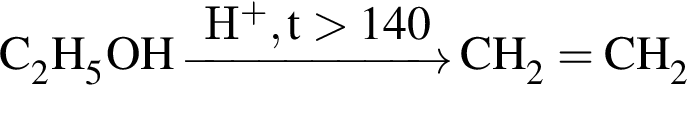


В результате реакции полимеризации, а не поликонденсации получают высокомолекулярное соединение:
Верным утверждением относительно бензола является:
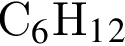
Вещества ![]() и
и ![]() в схеме превращений
в схеме превращений 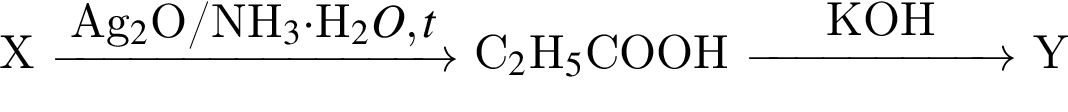 называются соответственно:
называются соответственно:
Органическое вещество ![]() полученное по схеме
полученное по схеме 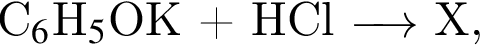 может реагировать в указанных условиях c:
может реагировать в указанных условиях c:
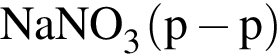
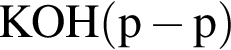
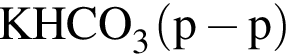
Для вещества справедливо утверждение:
Аминоуксусная кислота взаимодействует с веществами, формулы которых (электролиты взяты в виде водных растворов):
а) 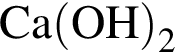 б)
б) 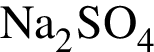 в)
в) 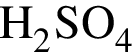 г)
г) ![]()
1) а, б
2) а, в, г
3) б, г
4) а, в
Укажите реагент, с помощью которого можно качественно отличить раствор уксусного альдегида от пропанола:
1) аммиачный раствор оксида серебра (I)
2) раствор гидроксида натрия
3) раствор хлорида железа (III)
4) раствор гидрокарбоната натрия
Установите соответствие между схемами превращений и реагентами X и Y. Все реакции протекают в одну стадию.
| Схема превращений | Реагент | |
|---|---|---|
| X | Y | |
| 1) H2/t Ni; | Br2O/t | |
| 2) H2/t, Ni | HBr | |
| 3) KOH; | H2SO4 (разб.) | |
| 4) K; | H2O | |
Запишите ответ в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А4Б1. Помните, что некоторые данные правого столбца могут не использоваться вообще.
В результате полного гидролиза дипептида, образованного 2-аминоэтановой кислотой, в присутствии избытка соляной кислоты получили только одно вещество — соль аминокислоты массой 53.52 г. Вычислите массу (г) дипептида, подвергшегося гидролизу.
Найдите сумму коэффициентов перед формулами сульфида калия и воды в уравнении реакции, схема которой
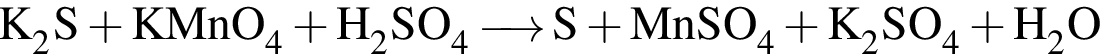
Сгорание водорода и метана протекает согласно термохимическим уравнениям:
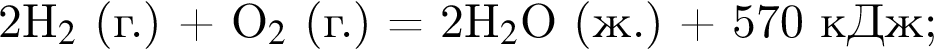
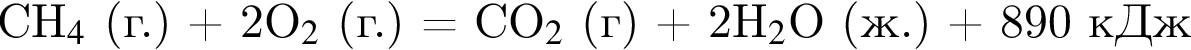
Рассчитайте количество теплоты (кДж), которая выделится при сгорании смеси водорода и метана массой 8 г, взятых в мольном отношении 2 : 1 соответственно.
Насыщенный альдегид, в молекуле которого содержится один атом кислорода, восстановили водородом. Продукт реакции восстановления прореагировал с уксусной кислотой в присутствии серной кислоты. В результате образовалось органическое соединение массой 42.24 г, при взаимодействии которого с избытком раствора гидроксида калия получилось калийсодержащее вещество массой 47.04 г. Определите молярную массу (г/моль) альдегида.
Масса соли, образовавшейся при взаимодействии алюминия с избытком концентрированного раствора гидроксида натрия, составила 2772 г. Рассчитайте химическое количество (моль) электронов, перешедших от атомов алюминия к атомам водорода в результате реакции.
Найдите сумму молярных масс (г/моль) медьсодержащего вещества В и цинксодержащего вещества Д в схеме превращений
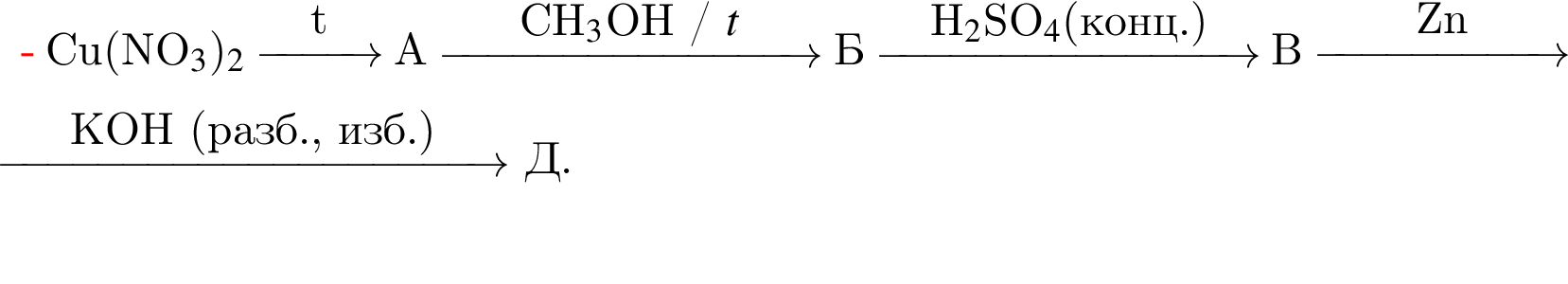
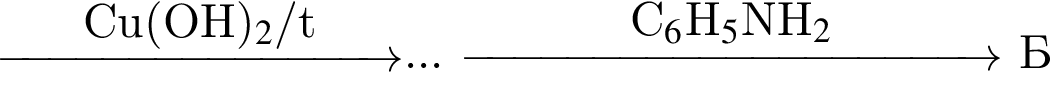
Найдите сумму молярных масс (г/моль) органических веществ ![]() и
и ![]() (вещество
(вещество ![]() имеет немолекулярное строение) в схеме превращений
имеет немолекулярное строение) в схеме превращений

Свинцовую пластинку массой 70 г опустили в раствор нитрата меди(II) массой 380 г. В момент извлечения пластинки из раствора массовая доля нитрата свинца в растворе оказалась равной 4,3 %. Вычислите, насколько процентов уменьшилась масса пластинки после извлечения ее из раствора.
Относительная плотность смеси озона и кислорода по гелию равна 9,2. Определите минимальный объем (дм3, н. у.) такой смеси, необходимой для полного окисления смеси этана, бутадиена-1,3 и бутина-2 масcой 105 г и относительной плотностью по неону 2,46.